腫瘤的遠程防禦系統: 淺談外泌體
戴廷浩 業務主任
樂斯科生技(股)公司
前言
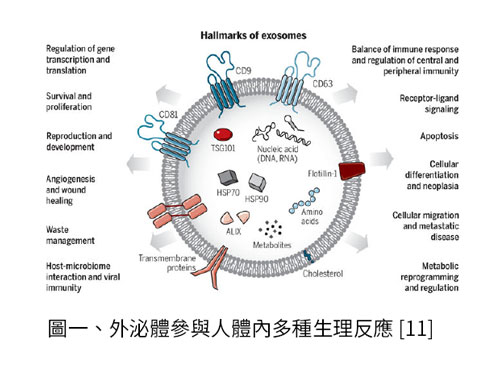
外泌體 (exosome) 是奈米級的生物囊泡,像是人體內的貨車,可攜帶蛋白質、脂質和核酸等細胞特異性物質,釋放到周圍的體液中,被鄰近或遠處細胞選擇性地吸收,為細胞間物質與訊號傳遞的關鍵介質,近年來更發現參與各種生理和病理過程 (圖一)[1]。外泌體的生合成 (biogenesis) 包含四個關鍵步驟,包括分子分選 (cargo sorting)、MVB (multivesicular body) 形成 (MVB formation) 和 MVB 的成熟 (maturation)、轉運 (transport of MVBs) 以及 MVB 與質膜的融合 (MVB fusion) [2]。每個過程都透過多種機制的競爭或協調,從而對不同的分子進行分類,進入不同的外泌體亞群,使外泌體具有高度異質性。但令人吃驚的是,癌細胞竟能利用各種策略,例如異常基因表達、翻譯後修飾和信號改變途徑,以調節外泌體的合成、組成和功能,進而促進癌症發展 [2]。因此了解外泌體,進一步探討外泌體產生機制及其在癌症的相關性,將有助於發展癌症治療策略。
外泌體簡介
外泌體是直徑約 30 – 150 nm 的細胞外囊泡 (extracellular vesicles), 由具有質膜的多囊泡體 multivesicular body (MVB) 所分泌。外泌體於 1983 年首次於綿羊網織紅血球細胞 (reticulocyte) 中被發現,1987 年正式命名為外泌體 (exosome)。2013 年諾貝爾生理學或醫學獎頒給 James E. Rathman、Randy W. Schekman 、Thomas C. Südhof 三人,表彰解開人體細胞如何調節傳輸系統之謎,讓科學家更加重視外泌體相關研究。而外泌體存在體液中包跨血液、唾液、尿液及母乳,且幾乎所有的細胞都能分泌,並隨著循環系統傳遞到其他遠處的細胞或組織進行調控並參與生理機轉。
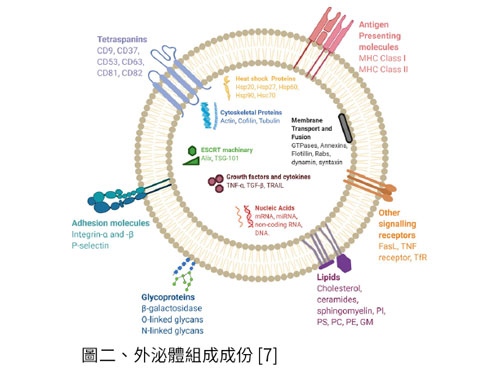
外泌體組成
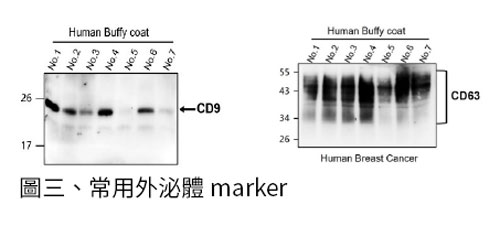
外泌體的組成成分 (圖二) 依據細胞類型及來源而不同,但主要的蛋白可分為四類:(A). 四跨膜蛋白 (Tetraspanins ): CD9, CD63, CD81和CD82、(B). 細胞內轉運蛋白 (Membrane transport and fusion) :Flotillin, Rab 和 Annexins、(C). 細胞骨架蛋白 (Cytoskeletal protein): actin, cofilin 和 tubulin、(D). 熱休克白 (Heat shock protein): HSP70和 HSP90。其中,常用的 marker 有 CD9、CD63 (圖三)、CD81、Alix 、TSG101、HSP27 等,運用抗體進行偵測,以進一步研究及診斷。除了上述蛋白外,外泌體也含有 DNA,miRNA 和 LncRNA 等核酸物質,可影響基因的表現,在腫瘤發展過程也扮演舉足輕重的角色 [1]。
外泌體的形成
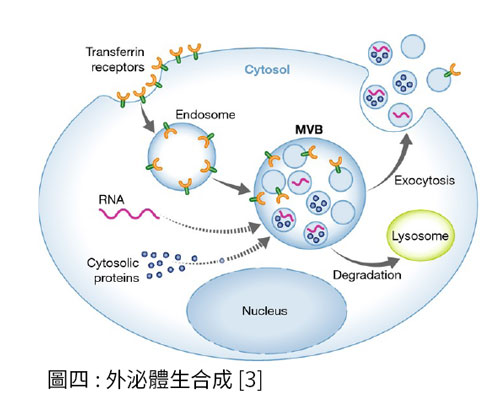
外泌體可以通過细胞外刺激、微生物攻擊和其他反應條件的誘導等而生成。目前研究認為,外泌體的形成步驟一開始细胞内陷形成早期内體,然後在內體轉運複合體及相關蛋白的參與調控下,形成多个個腔内小囊泡,接著在 RAB 酵素的調節下與细胞膜融合向細胞外分泌囊泡,即為外泌體 (圖四) [3]。
外泌體在癌症的應用
外泌體含有豐富的生物標記物可做為多種疾病診斷的生物指標,也可追蹤疾病進程。過去做癌症檢測常用螢光原位雜交 (FISH 及免疫組織染色 (IHC),然而外泌體存在於體液,帶有來源細胞的訊息,有助於病程追蹤監控,未來將有機會成為檢測的一大利器 [1]。
外泌體與腫瘤
免疫細胞可分泌外泌體毒殺癌細胞,如 Byeong-Cheol Ahn 等人利用小鼠模式動物發現自然殺手細胞的外泌體分泌 TNF-α,影響黑色素瘤細胞增生 [10]。而癌細胞所分泌的外泌體帶有腫瘤的抗原,當被樹突細胞捕獲時,也會激活免疫細胞,進行毒殺。
然而,近年來的研究也發現外泌體與腫瘤的關係不如我們想像的簡單,包含腫瘤生長、轉移、血管新生、腫瘤免疫調節及抗性,甚至許多研究發現癌細胞比正常細胞會分泌更多外泌體,其攜帶的核酸等物質會改變接收細胞的基因或蛋白表現,使正常細胞轉化成癌細胞 [8]。
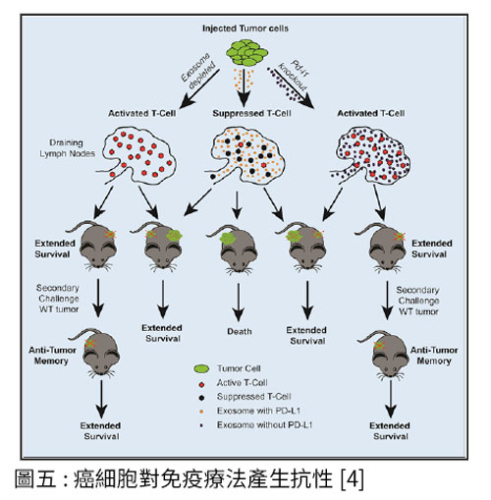
在腫瘤免疫的研究上也發現,癌細胞所分泌的外泌體包含許多的免疫抑制分子,抑制免疫細胞激活,躲過攻擊。2019 年 Mauro Poggio 等人以小鼠為模式生物,研究癌細胞對免疫療法產生抗性的原因,發現這些腫瘤細胞透過外泌體將 PDL1 帶到淋巴結中,使其可遠程抑制免疫細胞激活,進而對免疫檢查點藥物產生抗性 [4]。
而在, 黑色素瘤或前列腺癌也發現分泌的外泌體,其 FasL 誘導 Fas 依賴性 T 细胞凋亡 [9]。Chalmin 等 [5] 發現肺腺癌细胞分泌含 HSP72 的外泌體能激活 STAT3 信号通路而誘導 MDSCs 的免疫抑制作用。更多癌細胞透過外泌體生合成的調控如表一,外泌體為早期檢測的指標。
位在膜表面的蛋白可做為早期檢測的指標。2015 年 Raghu Kalluri[ 6] 在小鼠實驗及病人檢體研究中發現胰臟癌細胞的外泌體含有 Glypican 1,可進一步做為非侵入式診斷及早期檢測的標準。外泌體在細胞外環境的特性使其成為藥物運送或疾病分子的理想載體,可通過膜蛋白基因工程標的特定細胞類型或組織,一些以外泌體為基礎的藥物也進入臨床試驗階段,將來外泌體將更廣泛的運用在醫藥領域 [7]。
結語
最初認為外泌體只是细胞的廢棄物,然而外泌體能包裹包括脂質、RNA 和蛋白質等物質,在受體細胞或組織發出特定信號,使得外泌體在生理和生理上都扮演至關重要的作用。而外泌體幾乎存在於各種體液中,此特性也提供診斷的方便性,另一方面,外泌體具有攜帶物質的能力,對於如何應用外泌體作為藥物的遞送者也相當具有價值,綜合以上幾點特性使得外泌體成為潛在診斷的生物標誌物和治療疾病的工具。雖然臨床應用上外泌體的研究仍處於起步階段,需要進一步研究可大規模生產的外泌體及增加應用性,但毫無疑問的,外泌體仍是未來很有潛力的治療及診斷工具,並可能為目前面臨的各種醫學謎團提供解決方案。
參考文獻
- Cell Biosci. 2019 Feb 15;9:19.
- Mol Cancer. 2022 Nov 1;21(1):207.
- EMBO Rep. 2015 Jan;16(1):24-43.
- Cell. 2019 Apr 4;177(2):414-427.e13.
- J Clin Invest. 2010 Feb;120(2):457-71.
- Nature. 2015 Jul 9;523(7559):177-82.
- Cell Commun Signal. 2022 Sep 19;20(1):145.
- Int J Biol Sci. 2019 Jan 6;15(1):1-11.
- Cell Res. 2014 Oct;24(10):1164-80.
- heranostics. 2017 Jul 7;7(10):2732-2745.
- Science. 2020 Feb7;367(6478):eaau6977.